Jsou desettisíckrát tenčí než lidský vlas. Přesto je síla speciálních navovláken nepřekonatelná. Jediná injekce totiž dokáže přimět molekuly tančit a zvrátit dosud nevyléčitelnou paralýzu..
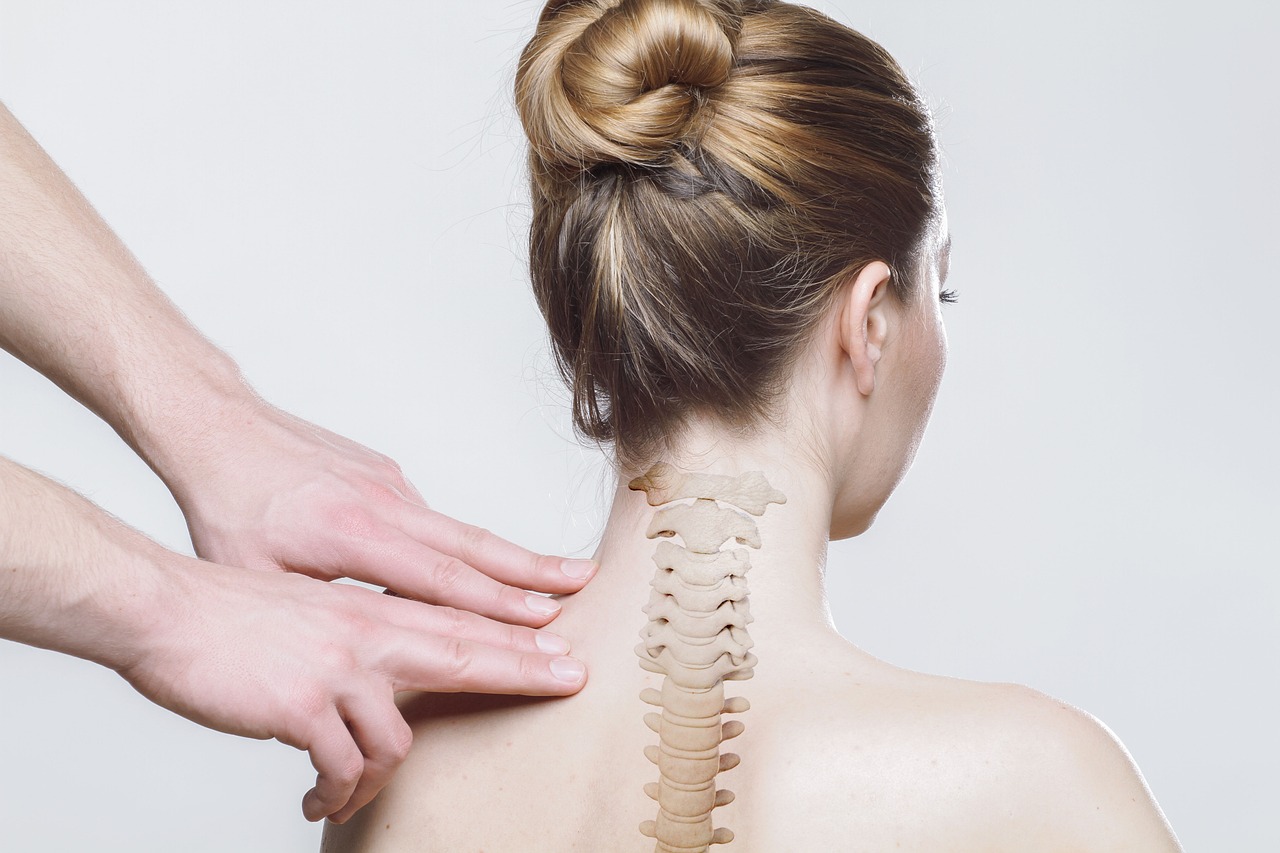
Ochrnutí patří i přes neustálé pokroky medicíny k závažným stavům s často nezvratnými následky. Jen ve Spojených státech sužuje poranění páteře na 380 000 lidí. Všem pacientům se však začíná blýskat na lepší časy.
Americkým vědcům ze Severozápadní univerzity v Illinois se totiž podařil malý zázrak – rozpohybovat paraplegické myši s pomocí gelu, který by brzy rádi otestovali i na lidech. Průlomový okamžik tým publikoval v odborném časopise Science.
Znovu v pohybu
Unikátní směs, jež se v organismu přeměnila na gel, vědci vstříkli do těla malým hlodavcům 24 hodin poté, co jim v narkóze přerušili míchu. Konkrétně se jednalo o aplikaci do tkání, které míchu obklopují.
A výsledek? Všem myším, jimž byla revoluční látka podána, se povedlo do čtyř týdnů od paralýzy začít zadní nožky znovu používat. K lepšímu pochopení funkčnosti byla provedena také pitva, která odhalila, že se přeťaté spoje nervových buněk v páteřích postupně zregenerovaly. Hlodavci, kteří lék nedostali, zůstali nadále paralyzovaní.
Splnit a zmizet
Tajemství úspěchu se podle vedoucího výzkumu Samuela I. Stuppa skrývá v nanovláknech. Ta posloužila k napodobení sítě molekul obklopujících tkáň, která je u zdravých jedinců zodpovědná za podporu buněk v míše.
Ale co víc. Léčivá látka značně ovlivňuje pohyb molekul. Dalo by se říci, že je nutí „tančit“, díky čemuž se mohou molekuly lépe zapojit do neustále se pohybujících buněčných receptorů. Pokud totiž tančí kolem vláken, či z nich vyskakují, pravděpodobnost, že se setkají s příslušnými receptory, se zvyšuje.
Výhodou unikátní látky je také její biologická odbouratelnost. Poté, co splní svou reparační funkci, se během 12 týdnů změní na živiny pro jednotlivé buňky, dokud z těla postupně zcela nevymizí. „Poranění míchy je velkou výzvou pro vědu po celá desetiletí. Jsem proto extrémně nadšený a věřím, že naše léčba pacientům pomůže,“ uvedl.
Extrémní senzace
„Hodláme jít přímo za Úřadem pro kontrolu potravin a léčiv (FDA), abychom co nejdříve zahájili proces schválení naší terapie a umožnili tak užití i lidským pacientům,“ dodal. Americký vědec apeluje především na skutečnost, že nervový systém u savců je velmi podobný hlodavcům, a na smutnou realitu, že aktuálně není možné ochrnutým pacientům jakkoli pomoci.
Souboj receptur?
Američtí odborníci přitom nejsou jediní, komu se v loňském roce podařilo zdolat dosud nezdolané. V rámci výzkumu totiž zabodoval i tým z Ruhr-Universität Bochum v Německu, kterému se za zdmi univerzity podařilo vytvořit signální protein hyper-interleukin-6. Ten následně vědci vstříkli do mozku pokusných, ochrnutých hlodavců.
Látka nejenže stimulovala jejich nervové buňky a donutila je k regeneraci, ale zároveň s nimi jakoby sdílela recept na tvorbu chybějících speciálních bílkovin. „Jedná se o tzv. designový cytokin, což znamená, že se v této podobě v přírodě nevyskytuje a musí být vyroben pomocí genetického inženýrství,” popsal autor studie Dietmar Fischer.
Stalo se (ne)možné
„Léčba genovou terapií pouze několika neuronů stimulovala axonální regeneraci různých nervových buněk v mozku a několika motorických traktů v míše současně,“ dodal. To umožnilo ochrnutým zvířatům chodit po 2–3 týdnech od podání.
Podle Fischerových slov byl celý tým kladnou reakcí zvířat na podaný lék velice překvapen. Až dosud totiž nic podobného nebylo možné.
A co bude dál?
Nyní se Fischer se svými spolupracovníky zaměřil na to, do jaké míry je možné tento, či podobný přístup zkombinovat s dalšími opatřeními k optimalizaci podávání hyper-interleukinu-6. A zda je možné dosáhnout lepších a rychlejších výsledků.
Předmětem dalších zkoumání se stane také fakt, zda protein bude mít pozitivní účinky na laboratorní myši i po několika měsících od podání.