Dlouhodobá remise HIV u něj trvá už 20 měsíců od doby, co mu byla provedena transplantace krvetvorných buněk a poté vysazena léčba antiretrovirotiky. Na rozdíl od předešlých pěti případů však dárce neměl vzácnou genetickou rezistenci vůči HIV..
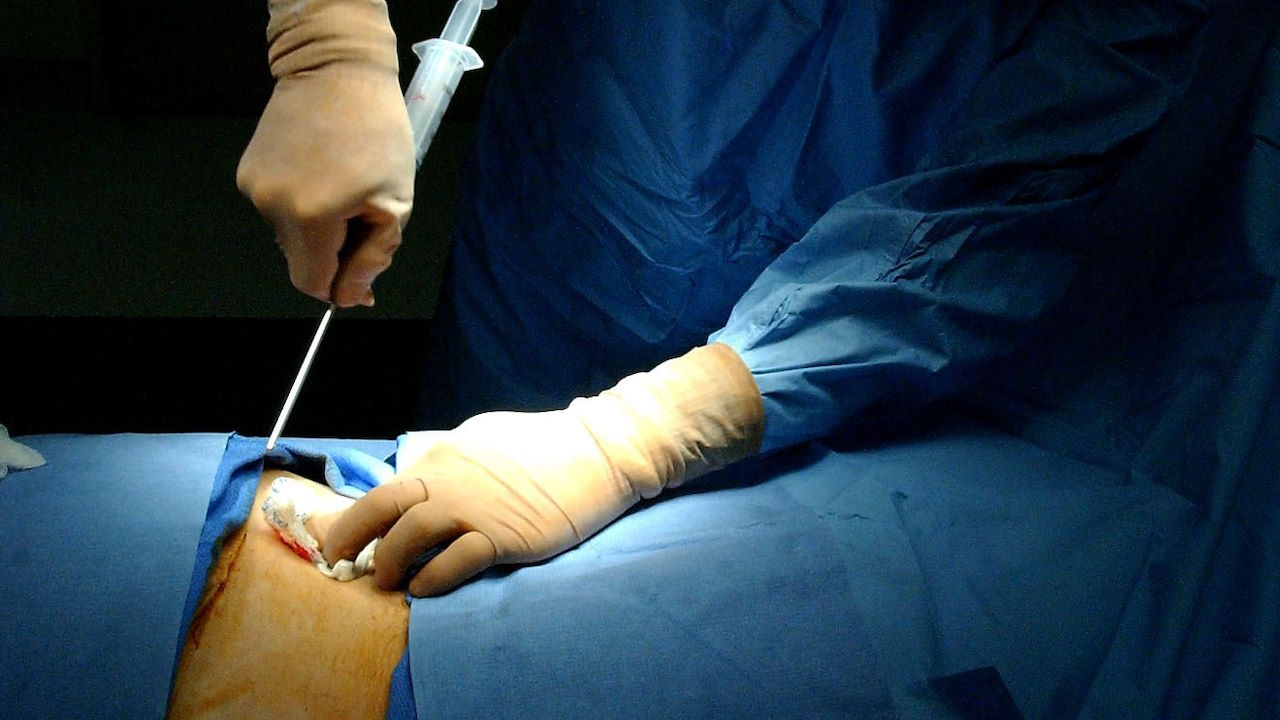
Muž, kterému se přezdívá „ženevský pacient“ podle města, ve kterém podstupoval léčbu, žil s virem HIV v těle od roku 1990. Následně začal v roce 2005 podstupovat tak zvanou antiretrovirovou terapii (ART), která měly virus potlačit a zabránit jeho postupu směrem k AIDS. Později se u něj rozvinula agresivní a vzácná forma rakoviny krve známá jako extramedulární myeloidní tumor, proto v roce 2018 podstoupil nejprve ozařování, poté chemoterapii a následně transplantaci krvetvorných buněk k léčbě tohoto stavu.
Potud se jeho příběh neliší od předchozích pěti pacientů, kteří rovněž trpěli HIV i rakovinou krve a k léčbě leukémie podstoupili transplantaci krvetvorných buněk, čehož lékaři úspěšně využili i k léčbě HIV. Podařilo se jim to díky tomu, že jako dárce nalezli člověka, který měl vzácnou genetickou mutaci rezistentní vůči HIV. Tato mutace se nazývaná CCR5-delta32. Gen CCR5 kóduje receptory na povrchu bílých krvinek.
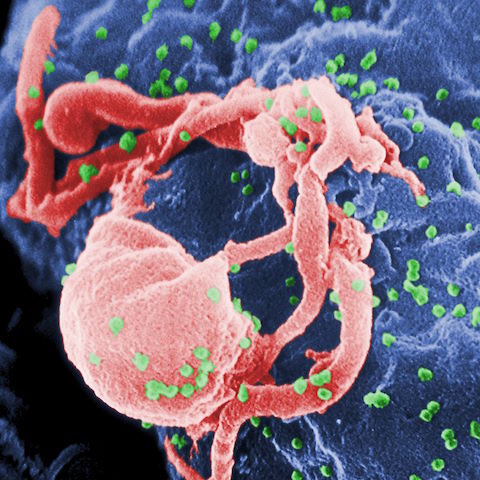
Za pomoci tohoto receptoru může do bílých krvinek vstupovat vir HIV, množit se v nich, a způsobit tak onemocnění AIDS.
Zázračná mutace delta32
Již před lety však bylo objeveno, že mutace delta 32 v CCR5 receptoru způsobuje jeho odlišnou stavbu, takže jím vir HIV nemůže do imunitní buňky prostoupit. Mutace delta 32 je rozšířená pouze u Evropanů, přičemž u severních národů je častější než u jižních.
V ČR je asi 1 % lidí, kteří jsou pro mutaci delta 32 homozygotní, to znamená, že tuto mutaci zdědili jako od otce, tak od matky a všechny jejich bílé krvinky tak mají receptor s mutací delta 32. U nich je téměř nulové riziko, že se v jejich těle virus HIV rozmnoží.
Dále asi 20 % české populace je pro mutaci delta 32 heterozygotní, to znamená, že zdědili mutaci pouze od jednoho z rodičů, takže polovina jejich bílých krvinek má receptor CCR5 „zdravý – wild type“ a polovina s mutací delta 32. Když se transplantát plně odolný vůči HIV ocitne v těle pacienta, nahradí jeho imunitní buňky zranitelné vůči HIV těmi odolnými, které virus nemůže napadnou.
Díky tomu se virus v těle pacienta nemá šanci již dále množit, ten tedy vstoupí do remise a může u něj být pozastavena léčba ART.
Dárce nebyl ideální
Ovšem v případě „ženevského pacienta“ nebyl vhodný dárce s mutací CCR5-delta32 nalezen, i když se o to vědci pokoušeli. Asier Sáez-Cirión, který se zabývá výzkumem virových rezervoárů a imunitní kontroly organismu na Pasteurově institutu v Paříži a který dohlížel na případ „ženevského pacienta“, k tomu říká:
„Skutečně došlo k pokusu najít kompatibilního dárce s CCR5-delta 32, což se však nezdařilo. Našli jsme však dárce heterozygotního. A protože prioritou byla léčba hematologického onemocnění, rozhodli jsme se přistoupit k transplantaci krvetvorných buněk od tohoto dárce.“.
Měsíc po transplantaci se počet buněk infikovaných virem HIV v těle padesátiletého muže prudce snížil a nebylo možné detekovat ani žádné protilátky proti viru. Na základě toho byla u „ženevského pacienta“ postupně zjednodušena jeho ART, snížil se počet léků ze tří na jeden.
Zcela ukončena mu pak antiretrovirová terapie byla v listopadu 2021. Nyní je již 20 měsíců bez léčby, aniž by došlo k návratu viru HIV. Stále je však možné, že muž v těle uchovává nějakou buňku infikovanou životaschopným virem, ta by totiž mohla v budoucnu „vyrazit do akce“ a znovu osídlit tělo virem HIV.
Co vedlo k remisi?
Lékaři spekulují nad tím, jak je možné, že u „ženevského pacienta“ došlo k možnému vyléčení, když u obdobných případů z minulosti došlo k návratu viru HIV do deseti měsíců po transplantaci od dárce bez mutace delta 32. Mají několik hypotéz.
Dr. Steven Deeks, přední výzkumník léčby HIV na Kalifornské univerzitě v San Franciscu, se domnívá, že k tomu mohla přispět chemoterapie, kterou pacient podstoupil, a také opakované epizody toho, co se nazývá reakcí štěpu proti hostiteli, při které T buňky nového imunitního systému rozpoznají buňky příjemce jako cizí a napadnou je, což způsobí válku mezi „štěpem“ a „hostitelem“.
Deeks k tomu poznamenává: „Nově vybudovaný imunitní systém mohl napadat a čistit starý imunitní systém, včetně jakýchkoli zbytkových T buněk přechovávajících HIV.“.
Sáez-Cirión podotýká, že je také možné, že imunosupresivní léky, které „ženevský pacient“ nadále dostává k prevenci reakce štěpu proti hostiteli, mohou bránit replikaci jakéhokoli reziduálního HIV. Jeho případ každopádně dává naději obdobně nemocným, že remise HIV muže být po transplantaci dosaženo, a to i bez pomoci mutace CCR5-delta 32. „Prostřednictvím této jedinečné situace prozkoumáváme nové cesty v naději, že remise nebo dokonce vyléčení HIV už jednoho dne nebude jednorázovým jevem,“ dodává Dr. Alexandra Calmyová, ředitelka oddělení HIV/AIDS v Ženevské univerzitní nemocnici.