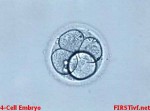
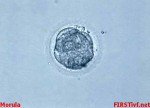
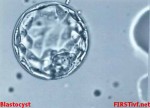
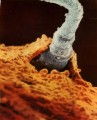
Lidstvo, poznamenané negativními dopady civilizace, má s plozením dětí stále větší potíže. Jako houby po letním dešti rostou na celém světě kliniky provozující asistovanou reprodukci, tedy rozmnožování s dopomocí lékařů«.
Vše začalo pozdě v noci 25. července 1978, když se v anglickém Manchesteru narodila Louise Brownová. Do dějin medicíny se zapsala tím, že byla počata poté, co embryolog Robert Edwards smísil v laboratoři v živném roztoku spermie pana Browna s vajíčky paní Brownové a gynekolog Patrick Steptoe přenesl vzniklé embryo do matčiny dělohy. Celý svět si tehdy kladl otázku: Co přijde dál? Pustí se odborníci do šlechtění inteligentních urostlých krasavců a krasavic? Nastala doba pro křížení lidí se zvířaty? Hrůzné vize se nenaplnily. Asistovaná reprodukce – odvětví humánní medicíny – přesto prodělalo ohromující proměny. „Komerční zájem klinik a vysoká poptávka ze strany neplodných párů vytvářejí celkem riskantní kombinaci, “ hodnotí současný stav asistované reprodukce britský odborník na léčbu neplodnosti Robert Winston z londýnské Imperial College.
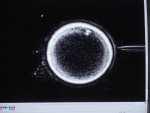
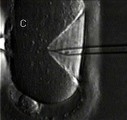
Spermie je v injekci
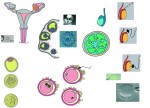
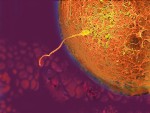
Nové techniky se v asistované reprodukci zavádějí závratnou rychlostí. Žádné odvětví medicíny jí v tom zřejmě nebude konkurovat. Názorným příkladem je postup označovaný jako intracytoplazmatická injekce spermie (zkratkou ICSI). Její princip byl odhalen víceméně náhodou v roce 1991, když se laborant jedné belgické kliniky pokoušel napomoci oplození tím, že spermii manžela pacientky vpravoval pomocí speciálních mikronástrojů pod ochranný obal vajíčka. To přitom nechtěně propíchl a spermii »vypustil« do jeho nitra. »Nehoda« měla překvapivý výsledek – vajíčko oplozené touto krajně násilnou cestou se normálně vyvíjelo. Rázem bylo jasné, že metoda ICSI nabízí šanci na otcovství i mužům, kterým tradiční »oplození ve zkumavce« nepomáhalo, protože jejich spermie nedokázaly samy do vajíčka proniknout. Téměř přes noc se dostala ICSI do nabídky většiny světových klinik. V USA se podílí z poloviny na všech výkonech prováděných v oboru asistované reprodukce. Rychlost nástupu ICSI do humánní medicíny byl zcela bezprecedentní. Zatímco klasické »oplození ve zkumavce« vědci po desetiletí piplali z dět ských nemocí na laboratorních zvířatech – myších, králících, křečcích, ICSI začala masově využívat humánní medicína v době, kdy u zvířat ještě nezaručovala spolehlivé výsledky. Například první makak rhesus (úzkonosá opice, využívaná k laboratornímu výzkumu), vzniklý pomocí ICSI, se narodil až v roce 2000.
Dnes už preferují bezpečnost
Bleskový nástup a nebetyčná popularita ICSI se výrazně podepsaly na zpoždění příslušných »bezpečnostních prověrek*. Ovšem nikoli všechny zprávy z dodatečně prováděných testů jsou příznivé. Britská epidemioložka Jennifer Kurinczuková z University of Leicester došla k závěru, že děti zplozené »ve zkumavce« trpí dvakrát častěji vrozenými defekty. Obdobná studie z USA států odhalila u takových jedinců nižší porodní váhu a vyšší pravděpodobnost úmrtí v prvním roce života. Praktici z klinik však s těmito závěry nesouhlasí. Navzdory všem problémům nemůžeme asistovanou reprodukci považovat za »psa utrženého ze řetězu«. V drtivé většině se »děti ze zkumavky« rodí zdravé a s přirozeně počatými vrstevníky si v ničem nezadají. Je jisté, že případ překotného zavedení techniky ICSI se už nebude opakovat. Například americký Úřad pro potraviny a léčiva vydal v roce 2001 nařízení, které podrobuje nově zaváděné postupy asistované reprodukce stejnému režimu prověrek, jakým procházejí například nové léky.
Narození více dětí není úspěchem
Lékaři a embryologové chtějí zdokonalit dosavadní postupy tak, aby se na minimum snížila zdravotní rizika, které asistovaná reprodukce přináší jak pro matku, tak i pro její děti. Proto se mj. omezuje počet zárodků, které jsou po oplození »ve zkumavce« přeneseny matce. Po stimulaci hormony může v matčině těle dozrát deset i více vajíček a lékaři často získají jejich oplozením větší počet embryí. Není divu, že se ocitají v pokušení přenést jich matce více, protože tím zvýší její naděje na otěhotnění. Pozor: Úspěšnost oplození ve zkumavce není závratně vysoká – pohybuje se kolem 30 %. S vyšším počtem přenášených embryí však zároveň stoupá pravděpodobnost, že se narodí dvojčata či trojčata. To je nežádoucí trend, protože těhotenství s více plody ohrožuje matku i děti. Odhaduje se, že náklady na lékařskou péči spojené s narozením dvojčat jsou v průměru desetkrát vyšší než náklady na narození jedináčka. U trojčat je to ještě mnohem vyšší
Přitom není nijak neobvyklé, když média 1 prezentují narození trojčat nebo čtyřčat po | asistované reprodukci jako »úspěch medicíny«. Měli bychom však spíše hovořit o vážném selhání, protože matka je mnohočetným těhotenstvím vystavena těžké zkoušce a na zdraví jsou ohroženy i její děti.
Gordický uzel rodinných vztahů
Oplození ve zkumavce umožnilo podstatně komplikovanější vztahy mezi »rodiči« a dětmi. Biologičtí rodiče nemusejí být totožní s rodiči »de iure«. V mnoha zemích je možné »dárcovství« pohlavních buněk nebo embryí a donošení dítěte »náhradní« matkou. K jednomu dítěti tak může vystupovat v nejrůznějších »rodičovských rolích« i pět dospělých lidí: Vajíčko daruje žena, která je biologickou matkou, a spermie daruje muž, který je biologickým otcem dítěte. Po »oplození ve zkumavce« může zárodek donosit najatá »náhradní matka« a porozené dítě pak vychovávají »adoptivní« rodiče – matka a otec »de iure«.
Budou se lidé přece jen klonovat?
V roce 2003 došel americký biolog Gerald Schatten k závěra, že stávajícími technikami nelze vytvořit klon opic ani člověka. Zjistil, že při tradičním postupu klonování ztrácí opičí vajíčko životně důležité bílkoviny, které potřebuje zárodek pro další zdárný vývoj. Bez těchto bílkovin dochází v buňkách klonu k vážným genetickým defektům. „Je to galerie genetické hrůzy,“ prohlásil Schatten Člověk má klíčové bílkoviny uloženy ve vajíčku a zárodku stejně jako opice makak a Schatten neviděl možnost, jak při klonování člověka zabránit jejich ztrátě. Tým čtrnácti vědců z Národní university v jihokorejském Soulu posílený o amerického biologa Josého Cibelliho ale usvědčil Schattena z omylu, když získal klonováním třicet lidských embryí a vypěstoval z nich buňky využitelné pro léčbu těžkých chorob. Korejci začali s 242 lidskými vajíčky získanými od 16 dobrovolnic. S nimi získali i tzv. kumulární buňky, které vajíčko chrání a vyživují. Z vajíček odstranili dědičnou informaci a tu nahradili dědičnou informací kumulární buňky. Vzniklá embrya byla klonem svých »předloh«.
Nahradí postižené části organismu
Pokud by je vědci přenesli ženám do dělohy, připojili by se k početnému zástupu šarlatánů, kteří koketují s klonováním lidí. Soulský tým se však vydal cestou tzv. terapeutického klonování. To si neklade za cíl narození lidského klonu. Má vyústit ve vznik buněk využitelných pro léčbu vážných chorob. Vědci ze soulské university v tomhle ambiciózním úkolu uspěli. Vypěstovali z buněk embrya »univerzální surovinu«, tzv. embryonální kmenové buňky, které se v laboratoři neomezeně množí a lze je změnou podmínek »pře-školit« na libovolné buňky těla. Schopnosti získaných buněk prověřili tak, že je voperovali do varlat myšáků s defektním imunitním systémem. V myším »živém inkubátoru« vznikaly například buňky lidské oční sítnice, kosti, chrupavky nebo svaloviny. Tak se nám otvírá cesta k tomu, aby lékaři jednou mohli vypěstovat pacientům náhradní buňky pro »opravu« infarktem poškozeného srdečního svalu, pro zhojení poraněné míchy či pro obnovu krvetvorby v nemocné kostní dřeni. Náhradní buňky přitom budou vypěstovány »přeškolením« vlastní buňky pacienta a jeho tělo je bez potíží přijme.
José Cibelli přesto varuje před přehnaným optimismem: „Naše práce přinese užitek až příštím generacím.“ Mnozí experti upozorňují i na odvrácenou tvář korejského úspěchu – akutní nebezpečí využití nových poznatků pro tvorbu lidských klonů.
Dočkáme se umělého vaječníku?
Budeme mít v dohledné době k dispozici »umělé varle« nebo »umělý vaječník«? Do těchto zařízení bychom na jedné straně vkládali buňky, odebrané z těla neplodných mužů či žen, a na druhé straně odebírali spermie či vajíčka pro početí dítěte ve zkumavce. »Umělé pohlavní žlázy« by vnesly revoluci do léčby vážných případů neplodnosti.
Pomohly by i pacientům, kteří absolvovali razantní léčbu rakoviny, po níž jim v pohlavních žlázách zanikly všechny pohlavní buňky. Až doposud se tito lidé museli smířit s doživotní neplodností. Rakovina varlat patří u mladých mužů k nejčastějším nádorovým onemocněním. Dospělým se nabízí možnost »odložit« si před léčbou spermie do tekutého dusíku a později je použít k početí potomka oplozením ve zkumavce. Malí hoši, jejichž varlata ještě spermie neprodukují, ale tuto šanci nemají. Podobné komplikace čekají i na ženy, kterým léčba nádorového onemocnění zničila v těle všechna vajíčka. Jejich situace bývá o to složitější, že mražení vajíček je podstatně komplikovanější než mražení spermií a jeho účinnost je velmi nízká. O tom, jak složitý úkol možné vytvoření »umělého varlete« nebo »umělého vaječníku« představuje, si uděláme představu, když si uvědomíme, že ani pro matku přírodu není tvorba spermií a vajíček jednoduchou záležitostí: Pohlavní buňky běžně vznikají v několika komplikovaných krocích a k úspěšnému završení vývoje potřebují dlouhé týdny a měsíce. Pohlavní buňka není na tento náročný úkol sama, protože jí vydatně pomáhají další buňky pohlavních žláz. Nahradit tuto dokonalou souhru v »umělé pohlavní žláze« znamená přímo nadlidský úkol.
Vajíčka a spermie ze zkumavky
Vaječníky samic obsahují tisíce buněk, které by se mohly nakonec vyvinout ve vajíčko schopné oplození. Drtivá většina z nich ale svůj vývoj nikdy nedokončí a bez užitku zanikne. Jedním z prvních biologů, jenž dokázal těmto vajíčkům pomoci uniknout nepřízni osudu kultivací v živných roztocích, byl americký biolog John Eppig z Jackson Laboratory. V roce 1996 získal myš oplozením vajíčka doslova vypiplaného z »nehotových« vajíček novorozené myšího mláděte. Tento myšák Eggbert (anglické »egg« znamená »vajíčko«) se stal mediální hvězdou. Bohužel svou slávu si dlouho neužíval: Záhy se ukázalo, že se narodil s těžkými defekty – včetně silné obezity. Bylo jasné, že John Eppig neposkytl myším vajíčkům vše, čeho se jim dostává v těle matky. Biologové se shodují v tom, že využití podobných postupů k léčbě neplodnosti by bylo nezodpovědným hazardem. Vajíčko je úžasně náchylné k poškozením, z nichž některá nedokážeme současnými laboratorními analýzami ani odhalit. „Naše kultivační postupy se neuvěřitelně zdokonalily. Ale k tomu, abychom dostihli o matku přírodu, máme ještě daleko,“ upřímně % přiznává John Eppig.
Myš funguje jako živý inkubátor
Někteří vědci se při pěstování vajíček uchylují ke »kukaččí strategii« a podstrkávají »ne-hotové« pohlavní buňky adoptivním pěstounům. Nejlépe se v této roli osvědčily myši, které mají kvůli poškození dědičné informace nefunkční imunitní systém. Když jim vědci vpraví do těla pohlavní buňky cizího živočišného druhu, myši »vetřelce« tolerují a vytvářejí jim jako živý inkubátor příhodné podmínky. V těle myší samice narostou vajíčka v kusu transplantované tkáně z lidského vaječníku a stejně zdatně si vedou i nehotové samčí pohlavní buňky v těle myšáků. Pro humánní medicínu je tento »pěstounský« systém zřejmě nepřijatelný, protože tu kromě jiného hrozí, že se k lidským pohlavním buňkám dostanou zvířecí viry. Pro reprodukci zvířat je však metoda velkým příslibem. Německá bioložka Ina Dobrinská působící na americké University of Pennsylvania už dokázala v těle myšáků vypěstovat spermie kozla, kance, makaka a v současné době nutí laboratorní myšáky produkovat spermie domácích kocourů. Tyto pokusy jsou jen průpravou pro pěstování spermií velkých kočkovitých šelem ohrožených vyhubením i jiných vzácných živočichů.
Lze oplodnit bez spermií?
Potřebujeme vůbec k rozmnožování pohlavní buňky? Ty mají sice ve srovnání s obyčejnými tělními buňkami jen polovinu dědičné informace, ale tahle »drobnost« se dá celkem snadno napravit: Nezralé vajíčko je k této nezbytné redukci dědičné informace předem naprogramováno. Co kdybychom mu podstrčili místo spermie jádro tělní buňky? Možná by si dědičnou informaci podvržené buňky zredukovalo a spermii by si z ní tak vyrobilo. Tento trik jako jedna z prvních odzkoušela australská bioložka Orly Lachamová-Kaplanová z melbournského Monash Institute of Reproduction and Development: Vpašovala do dělícího se vajíčka místo spermie tělní buňku myšího samce. Získala embrya, která se dále vyvíjela. Mláďata se z nich ale nenarodila!
Biolog Gianpietro Palermo z americké Cor-nell University zase podstrčil jádro tělní buňky za dědičnou informaci vajíčka. Vajíčko s ní naložilo jako se svou vlastní dědičnou informací a provedlo patřičnou redukci. Mláďata se po oplození takto získaných vajíček rovněž nenarodila a podle mínění řady světových expertů se ani nikdy nenarodí. Ukazuje se, že vajíčko neumí dědičnou informaci tělní buňky správně rozdělit a dopouští se přitom vážných chyb. Vzniklé embryo buď vůbec nemá šanci na zdárný vývoj nebo vkládá potomkovi do vínku vážný defekt. Není to jediné riziko, které číhá na tělní buňky přeměněné na buňky pohlavní. Tělní buňky utržily za svůj život nejeden šrám na dědičné informaci. Použít takto poškozenou dědičnou informaci pro početí dítěte by bylo šíleně riskantní.
Kaguya – tvor narozený bez otce
Záběry s myškou Kaguyou, která se nedávno narodila v laboratoři vědce Tomohira Kona z Tokijské zemědělské univerzity, obletěly celý svět. Obvykle je provázejí zprávy věštící zánik mužského pokolení. Tak jednoduché to ale není: Lidstvo se bez otců ještě dlouho neobejde! Tomohiro Kono vytvořil tuto myšku spojením dvou vajíček a na první pohled tak popřel biologické zákonitosti, které savcům zapovídají »neposkvrněné početí« bez účasti
otce. Náročné experimenty ale skončily úspěchem jen proto, že vědci zasáhli do dědičné informace jednoho z vajíček tak, že ho do značné míry »rekvalifikovali« na spermii. Vajíčka a spermie se liší spektrem »bdících« a »spících« genů. Tyto geny se musí v zárodku sejít v příslušné konstelaci, jinak živočich nemá šanci vůbec přijít na svět. Kono vlastně nahradil přirozené oplození vajíčka spermií za spojení »mateřského« vajíčka s vajíčkem »přestavěným« na spermii. „Technika je příliš komplikovaná. Je nemožné ji provést na člověku a já bych se o to ani nechtěl pokoušet. Na řadě je prase,“ prozradil Tomohiro Kono své nejbližší plány. V budoucnu se může situace změnit: Pokud se mnohonásobně zvýší jak úspěšnost, tak i bezpečnost postupu, možná se rejstřík technik pro léčbu neplodnosti nakonec rozšíří i o početí bez otce. Britský lékař Simon Fishel z Centra asistované reprodukce v Nottinghamu říká: „Například páry homosexuálních žen by spojením vajíček počaly dceru, která ponese dědičnou informaci obou partnerek. To je něco jiného než klonování, kde by narozené dítě bylo geneticky totožné jen s jedním člověkem.“
Zmrazíme životy pro lepší časy?
Bez vody nelze žít. Také všechny životní děje uvnitř buněk vyžadují vodu. Bez životadárné kapaliny se v buňce vše zastaví. Vědci toho mistrně využívají k tomu, aby zastavili čas.
Zmrazit buňku je celkem jednoduché. Mnohem obtížnější je to provést tak, aby buňka po rozmrazení opět ožila. O tom, že to jde, svědčí příklady z přírody. Například některé žáby přes zimu zmrznou doslova na kámen a tráví dlouhé měsíce v teplotách kolem 10 °C pod bodem mrazu. Na jaře během několika hodin zase rozmrznou a druhý den už se naplno věnují námluvám.
Číhají různá nebezpečí
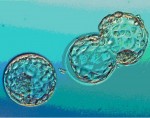
Při léčbě neplodnosti metodou oplození ve zkumavce nejednou vzniká mnohem více embryí, než kolik jich mohou lékaři matce přenést do dělohy. Co s těmi zbývajícími? Nabízí se možnost embrya zmrazit a uložit je do třeskutého mrazu -196 °C v tekutém dusíku. Tam mohou bez újmy trávit dlouhá léta.
Pokud by se rodiče rozhodli počít další děti, nemusejí již podstupovat celou proceduru oplození ve zkumavce, která zahrnuje i drahé a mnohdy nepříjemné hormonální ošetření matky. Stačí embrya v laboratoři rozmrazit, nechat je »vzpamatovat« v živných roztocích a přenést do těla matky.
Celý postup ale není tak jednoduchý, jak na první pohled vypadá. Mrazení, jaké známe z domácích mrazáků, znamená pro buňku jistou smrt. Hodně záleží na rychlosti, s jakou pří mrazení klesá teplota. Při rychlém ochlazení mrzne voda do velkých krystalů, které buňku roztrhají na kusy. Z pomalu ochlazované buňky uniká voda v kapalném skupenství a i toto »vysychání« mívá smrtící následky.
Jde o rozumný kompromis
Úspěšné mrazení buněk je uměním kompromisu, který představuje tempo poklesu teploty kolem 1 °C za minutu. Pro dodržení optimální rychlosti mrazení buněk se používají počítačem řízená automatická zařízení, kde teplotu v každém okamžiku hlídají citlivá čidla. Další trik spočívá ve využití ochranných látek, tzv. kryoprotektiv. Už od 40. let dvacátého století biologové vědí, že některé chemikálie dokážou buňku proti nepříznivým vlivům nízkých teplot obrnit. Proto se buňky mrazí v ochranných »koktejlech« obsahujících například glycerol, propandiol nebo dimethylsulfoxid. Ovšem kryoprotektiva jsou většinou toxická, a tak jsou biologové nuceni k dalším kompromisům: Koncentrace kryoprotektiv
musí být dost vysoká, aby se projevil ochranný efekt, a zároveň tak nízká, aby buňka kontakt s nimi bez větší úhony přežila.
Chybí bílkovina chránící před nádory
Biologové a lékaři postupují při mrazení s krajní opatrností. Přesto nemohou uchránit embrya před celou řadou nepříznivých vlivů. Nad mnoha z nich nemají nejmenší kontrolu a o jejich konkrétních následcích pro embryo se můžou jen dohadovat. Není divu, že se stále více vědců a lékařů zabývá biologickou bezpečností mrazení lidských embryí. Obavy jsou zřejmě namístě. Nedávno publikoval znepokojivé výsledky výzkumu v této oblasti britský odborník na léčbu neplodnosti Robert Winston. Dokázal, že mrazeným embryím mohou chybět některé velmi důležité molekuly. „Rozhodně nechci děsit rodiče dětí, které přišly na svět díky asistované reprodukci,“ tvrdí Winston. Zároveň však dodává, že podle jeho názoru nebyly některé techniky včetně mrazení embryí dostatečně otestovány.
Tuberin – velká neznámá pro embrya
Winston prověřoval u lidských embryí množství »suroviny« potřebné pro výrobu bílkoviny tuberinu, který se kromě jiného podílí i na dělení buněk. Zjistil, že některá embrya mají silně sníženou schopnost tvorby tuberinu. Je těžké odhadovat, co to pro mrazená embrya znamená. Tuberin patří k bílkovinám nezbytným pro ochranu lidského těla před nádorovým bujením. Nedostatek tuberinu vyvolává u dospělých lidí tzv. tuberózní sklerózu. Choroba postihuje nervovou soustavu a doprovází ji vznik nádorů v oku, mozku, ledvinách a dalších orgánech. Následky nedostatku tuberinu pro embryo neznáme. Bylo by proto nezodpovědné vyvozovat z Winstonovy studie závěr, že lidé narození z rozmrazených embryí čelí vyššímu riziku tuberózní sklerózy. Nedělá to ostatně ani autor studie. „Rozdíl mezi používáním nezmrazených a zmrazených embryí může být podobný, jako když vaříte ze zmrazených surovin místo z čerstvých,“ říká Winston a dodává, že bychom měli hledat metody zmrazování, které poškozují embrya co nejméně.
Projeví se následky mrazení až později?
Situace kolem mrazení embryí může být ještě složitější, než se nám to jeví ve světle studie Roberta Winstona. Tým francouzských vědců již před několika lety testoval, nakolik se projeví mrazení embryí na zdravotním stavu živočichů po dosažení pokročilejšího věku. Také tato studie zamotala vědcům hlavy. Myši, které se narodily ze zamrazených embryí, byly v mládí i »produktivním věku« v naprostém pořádku. Se stářím na ně však doléhalo mnohem více neduhů než na myši narozené z embryí ušetřených mrazivé životní etapy. Myši narozené ze zamrazených embryí v pokročilém věku výrazně tloustly. Zhoršené výsledky testů při hledání cesty laboratorním bludištěm signalizovaly snížený výkon mozku. Odchylky ve tvaru čelisti, který je dán vzájemnou souhrou asi stovky genů, zase naznačovaly, že mrazení poznamenalo i dědičnou informaci. Vznik těchto obtíží zjevně podmiňovaly dědičné sklony zvířat, protože některé genetické linie myší byly k následkům mrazení embryí poměrně odolné.
Budou embrya projednávat soudy?
Prvním lidem narozeným ze zmrazených embryí je dnes kolem dvaceti let. Drtivá většina z nich nemá žádné zdravotní potíže, které bychom mohli připsat na vrub tomu, že nejranější období života strávili jako několikabuněčné zárodky v tekutém dusíku. Snad to signalizuje, že člověk patří k živočišným druhům, na jehož embrya nemá mrazení tak negativní dopad jako na embrya myší. Ovšem nejen právní problém nastává ve chvíli, když muž a žena, kteří si nechali zmrazit embrya na pozdější dobu, se mezitím rozejdou! Víc ukáže čas!
MALÝ SLOVNÍK ASISTOVANÉ REPRODUKCE
Oplození in vitro
Latinské »in vitro« znamená doslova »ve skle«. Obvykle se za tímto slovním spojením skrývají laboratorní práce, při kterých objekty našeho zájmu (v případě oplození jsou to spermie a vajíčka) pobývají mimo tělo a jsou odkázány na umělé laboratorní podmínky. V češtině se někdy »in vitro« překládá jako »ve zkumavce«. Ovšem doby, kdy lékaři a biologové experimentovali s pohlavními buňkami ve skleněných zkumavkách, jsou už historií. Dnes se pro oplození in vitro používá speciálních misek vyrobených ze zvláštních plastů.
Mikromanipulátor
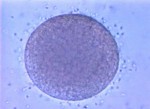
Vajíčko člověka měří v průměru jen o málo více než 0,1 mm. Takový objekt je vidět jen pod mikroskopem a zasahovat do něj nelze nástrojem drženým »holou« rukou. Například pro vstříknutí spermie neplodného muže do vajíčka se používají tzv. mikromanipulátory, které převádějí jemné pohyby ruky embryologa na ještě jemnější pohyby mikronástrojů. Navíc se použitím mikromanipulátoru zbavíme třesu, který práci lidské ruky nevyhnutně provází.
Mikroinjektor
K nasátí spermie do jemné kapiláry a jejímu I vstřiknutí do I nitra oplozováného vajíčka potřebuje embryolog velice jemnou »injekční stříkačku« – tzv. mikroinjektor. Toto zařízení dokáže nasát do jemné kapiláry spermii s kapičkou živného roztoku o objemu několika mála pikolitrů (1 pikolitr = 0,000001 krychlového milimetru).
NĚKTERÉ TECHNIKY ASISTOVANÉ REPRODUKCE
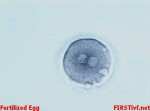
IVF – in vitro fertilizace (česky »oplození ve zkumavce«)
Z vaječníků nastávající matky jsou odebrána vajíčka, která dozrála po podání hormonálních léků. Vajíčka se v živ-
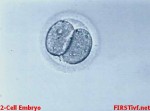
ném roztoku smíchají se spermiemi otce a tam také dojde k oplození. Vzniklé zárodky se vyvíjejí 2-3 dny v laboratoři, poté jsou dva až tři nejživotaschopnější přeneseny do dělohy matky.
SUZI – subzonální inseminace
Někdy je bílkovinný ochranný obal vajíčka (tzv. zona pellucida) pro spermii příliš pevný a ta přes něj nedokáže proniknout. Pak pomůže embryolog v laboratoři spermiím tím, že je vstříkne pod bílkovinný obal. Do vajíčka pak už spermie proniknou samy.
»Zona drilling« (česky přeložitelné jako »navrtání zony pellucidy«)
V příliš pevném obalu vajíčka embryolog v laboratoři vytvoří otvor
(mechanicky skleněnou jehlou, chemicky kyselým roztokem nebo i laserem) a teprve pak vajíčko podrobí »oplození ve zkumavce«. Spermie má možnost »pro-lézt« k vajíčku připraveným otvorem.
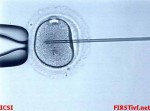
ICSI – intracytoplasmic sperm injection (česky intracytoplazmatická injekce spermie)
Spermie, které by samy do vajíčka nikdy nepronikly, jsou do jeho nitra vstříknuty jemnou skleněnou kapilárou.
ROSI – round spermatid injection – injekce okrouhlých spermatid
U mužů, v jejichž varlatech vůbec nevznikají spermie, lze pro oplození použít »nehotové« pohlavní buňky, tzv. spermatidy. Ty jsou vstříknuty do vajíčka jemnou skleněnou kapilárou a vyvíjející se zárodek je přenesen matce.
Transplantace cytoplazmy vajíčka. Především vajíčka starších žen často nejsou schopna zajistit zdárný vývoj po oplození spermií. Proto je jim provedena »transfuze« cytoplazmy. Zhruba desetina objemu vajíčka je na-
hrazena cytoplazmou odebranou z vajíčka poskytnutého zdravou dobrovolnou dárkyní. To stačí, aby vajíčko získalo potřebnou životaschopnost.
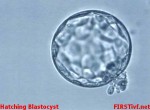
Asistovaný hatching. Po oplození se embryo vyvíjí několik dní uvnitř bílkovinného obalu vajíčka. Pro spojení s dělohou matky se ale musí z tohoto obalu vymanit. »Vylézání« z obalu se říká »hatching«. Termín je odvozen od anglického »hatch« čili »klubat se«. Po oplození »ve zkumavce“ může být embryo příliš slabé, než aby stěnu obalu prolomilo a uvolnilo se. Embryolog mu proto pomůže tím, že obal v jednom místě naruší. |
JAK VZNIKÁ VAJÍČKO – PŮLSTOLETÍ OMYLŮ
Americký biolog Jonathan Tilly vyvolal převrat v biologii. Šokoval odborníky, kteří padesát let věřili, že vajíčko u savců vzniká v raných stadiích vývoje budoucí matky – v době, kdy se ona sama ještě vyvíjí jako plod. Celou tu dobu si vědci mysleli, že ze zásoby jednou provždy vytvořených vajíček po celý život už jen ubývá. Dvacetitýdenní lidský plod ženského pohlaví si vytvoří v pohlavních žlázách asi 7 milionů vajíček. Právě narozené děvčátko si jich přináší na svět 3 miliony a dívka v pubertě jich má k dispozici »jen« 300 tisíc. Každý pohlavní cyklus zahájí přípravu na uvolnění z vaječníku a následné oplození asi 15 vajíček. Jen jedno z nich tuto průpravu dokončí a má šanci proměnit se po oplození spermií na lidský zárodek. Zbývající vajíčka zanikají. Na věčnost se neustále odebírají i vajíčka, která cestu k početí nového života vůbec nezahájila. Nakonec se zásoba pohlavních buněk vyčerpá a tím hasnou naděje na zplození vlastního potomka. U člověka k tomu dochází mezi čtyřicátým a padesátým rokem.
Ovšem expert Tilly dokázal, že všechno je úplně jinak: Ve vaječnících dospělých myší je asi 5000 vajíček a více než čtvrtina z nich se nachází »ve stadiu pokročilého rozkladu«. Během pouhých tří dnů po nich nezbude ani stopy. Pokud by platila klasická představa, udržela by si myší samice plodnost nejvýše pár týdnů a pak by zásobu vajíček vyčerpala. Jenže myší samice může mít mláďata i ve stáří jednoho roku! „Nabízelo se jediné pravděpodobné vysvětlení. I dospělá myš si vytváří nová vajíčka,“ říká Jonathan Tilly. Svou kacířskou myšlenku podpořil přesvědčivými důkazy. V každém vaječníku dospělé myši narazil na sedmdesát zvláštních buněk, které se neustále dělí. Část se mění na vajíčka, zbytek zůstává »buněčnou surovinou« a je připraven celý proces kdykoli zopakovat. Právě tyto buňky se starají, aby ve vaječníku vznikala stále nová a nová vajíčka.
„Jsou to zcela zásadní poznatky, které mohou v našem oboru všechno změnit,“ říká Tilly.
Léčbě neplodnosti se Tillyho objevem otevírá zcela nové pole působnosti, o jehož existenci neměli lékaři dosud ani potuchy: U člověka zřejmě nečekají vajíčka vytvořená plodem dlouhá desetiletí na to, zda z nich oplozením vznikne nový jedinec. Co to znamená? Dítě může být počato z vajíčka, které před několika týdny či měsíci v těle jeho matky ještě vůbec neexistovalo. Mnoho případů neplodnosti proto zřejmě vyvolají poruchy tvorby nových vajíček, a nikoli zvýšené tempo jejich zániku.