Když se řekne „atom“, naprosté většině lidí vytane na mysli malá sluneční soustava, tzv. Rutherfordův model. Možná kvůli tomu, že je všudypřítomný – esteticky rozvířené elektrony se staly symbolem ateistů, Mezinárodní agentury pro atomovou energii i TV seriálu Teorie velkého třesku.
A to navzdory tomu, že je vadný – svět na něm vystavený by zkolaboval do 10 sekund.
„Na Novém Zélandu nemáme peníze, tak musíme přemýšlet,“ opakoval často Ernest Rutherford (1871–1937) po svém otci. Poslouchat rady rodičů se farmářskému chlapci, který se narodil 15 mil od nejbližší vesnice, vyplatilo.
Stal se vědeckou živoucí legendou, byl vyznamenán Nobelovou cenou za chemii, uveden do stavu šlechtického, a když zemřel, jeho popel uložili na Westminsterské opatství vedle anglické smetánky. Ani zakladatel jaderné fyziky a duchovní otec atomové fyziky se ovšem neubránil šlápnutí vedle.
Rozinky v pudingu
Svět, do kterého se Rutherford narodil, se zásadně lišil od toho, který opouštěl. Země existovala jen 100 milionů let a atom, základní částice přírodního světa, byla biliardová koule – pevná a nedělitelná sféra.
Tak to alespoň stálo v učebnicích ještě začátkem 20. století. Byl to Rutherford, kdo postavil obě tyto domněnky na hlavu. Už v roce 1904 přišel se svým tzv. „pudinkovým modelem atomu“ britský fyzik Joseph John Thomson (1856–1940).
Podle něj se hmota rovnoměrně rozprostírala napříč celým atomem a elektrony v něm byly rozesety jako rozinky v anglickém vánočním pudingu, odtud také jeho název. V době, kdy se Rutherford už coby profesor Viktoriiny univerzity v Manchesteru začal zabývat studiem organizace atomu, byl subatomární svět vánočním pudingem a vše se zdálo v nejlepším pořádku.
Pak ale přišlo léto roku 1909 a slavný experiment mladých profesorových asistentů, při kterém náhodou objevili atomové jádro.
Experiment nad zlato
To ale zatím Hans Geiger (1882–1945) ani Ernest Marsden (1889–1970) nemohli tušit. V rámci experimentu pálili z ocelové krabičky paprsek částic alfa do vakuové komory přes zlatou fólii tenkou 6/100 000 cm, tedy asi jako 400 atomů naskládaných za sebe.
Pokud by platil Thomsonův pudinkový model, alfa částice by musely projít skrze fólii beze změny trajektorie. U většiny tomu tak skutečně bylo. Pár jich ovšem po průchodu fólií výrazně změnilo směr a jedna z 8 000 částic se dokonce vrátila zpátky, odkud vylétla, jako by ji odrazila nějaká neprostupná bariéra.
To mladé vědce i profesora zarazilo. K vychýlení částice alfa, která cestovala sedminovou rychlostí světla, by bylo potřeba miliardy voltů. „Stala se ta nejneuvěřitelnější událost v celém mém životě,“ napsal si tehdy konsternovaný Rutherford, „bylo to stejně nepravděpodobné, jako kdyby se 15palcová dělová koule vystřelená proti listu papíru od něj odrazila a trefila střelce.“.
I na ničem záleží
Profesor se uchýlil ke strategii, která se mu osvědčila už tolikrát předtím – dlouze se zamyslel. Uvědomil si, že částice alfa musely narazit na něco nesrovnatelně hmotnějšího než ony samy. „Tehdy mě napadla představa atomu s těžkým malým jádrem nesoucím náboj,“ vzpomínal profesor.
Thomsonův model se ukázal jako neplatný. Konečně v roce 1911 se zjevil v Geigerově laboratoři a docela prostě mu oznámil: „Už vím, jak vypadá atom.“ Jeho nový model atomu vodíku, založený na Geigerově-Marsdenovu experimentu, z větší části neobsahoval nic – jen pár elektrických částic obíhajících ve vakuu kolem velmi hmotného jádra, podobně jako planety kolem slunce.
Nově objevené jádro, jehož relativní velikost vypočítal na jednu biliontinu palce, okupovalo pouze jednu miliardtinu prostoru atomu. „Byla to velikost špendlíkové hlavičky v centru Katedrály svatého Pavla, obsahovala ovšem 3 999/4 000 hmoty atomu,“ napsal v Rutherfordově biografii americký autor Richard Reeves.

Vady na kráse planetárního modelu
Ačkoliv Rutherfordův model atomu vodíku byl krokem vpřed, stále narážel na několik fyzikálních problémů. Náš planetární systém udržuje pohromadě gravitace. Vnitřek atomu, který obsahuje nabité částice, se ale řídí jinou silou, tzv.
Coulombovým zákonem. Víme také, že objekt pohybující se v kruzích díky dostředivé síle neustále zrychluje. Podle klasické elektromagnetické teorie vyzařují zrychlující nabité částice radiaci ve formě elektromagnetických vln.
Tím postupně přicházejí o energii. Pokud by měl Rutherfordův model platit, vzdálenost elektronu od jádra by se zákonitě musela neustále zmenšovat až do chvíle, kdy by se elektrony zřítily do kladně nabitého jádra. To by znamenalo, že atomy vodíku by měly životnost zhruba 10 sekund.
Nadějný studentík
Profesor Rutherford si byl plně vědom toho, že jeho model je nestabilní. Podporoval proto všechny snahy o vyřešení této záhady, mezi nimi také úsilí svého stážisty z Dánska, Nielse Bohra (1885–1962). Říká se, že Bohr se stal Rutherfordovy synem, kterého nikdy neměl.
Vzájemný obdiv, přátelství a spolupráce vytrvala až do konce života. „Bohr byl také možná jedinou osobou na světě, která mohla přesvědčivě stabilizovat Rutherfordův model,“ napsal Reeves. Za pomocí kvantových teorií Maxe Plancka modifikoval základní model svého učitele.
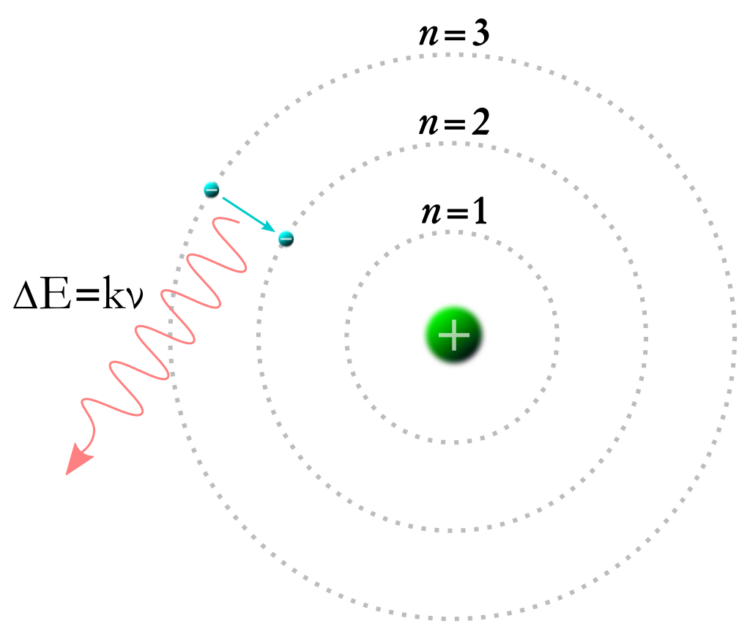
Bohr spočítal, že elektrony absorbují vnější energii vstupující do atomu, jako je světlo nebo radioaktivní teplo. To jim spolu s odstředivou silou brání ve zřícení se do jádra. Bohrův model atomu z roku 1913 vysloužil fyzikovi v roce 1922 Nobelovu cenu.
A to navzdory tomu, že ani tento pokus nebyl bez chyb – už za 12 ho nahradil přesnější kvantově mechanický model atomu. Přesto Bohrův model vedl k širokému spektru přesných předpovědí a nových objevů: od předpovězení výsledků chemických reakcí, k určení složení vzdálených hvězd k vytvoření atomové bomby.