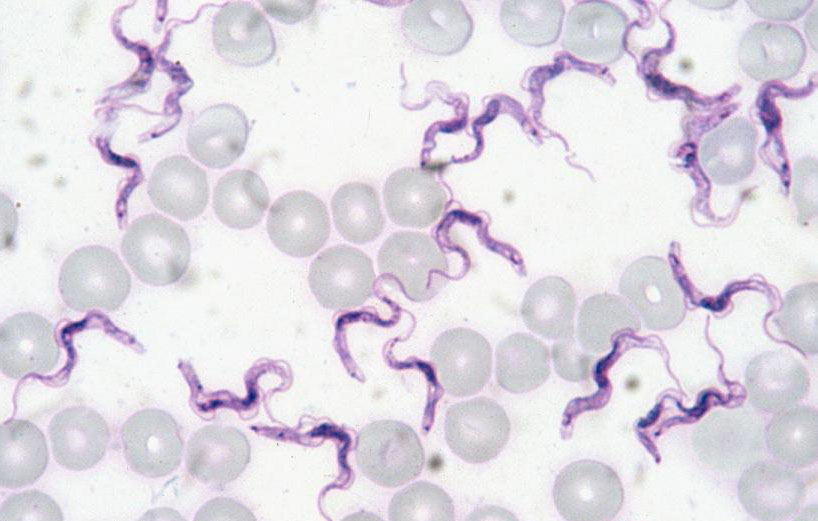
Parazitologové z Biologického centra AV ČR společně s vědci z Cambridgeské univerzity, mezi nimiž byl i nositel Nobelovy ceny za chemii z roku 1997, John E. Walker, rozluštili strukturu mitochondriálního podkomplexu tzv.
F1-ATPázy u jednobuněčného parazita Trypanozomy spavičné (Trypanosoma brucei). Ten způsobuje spavou nemoc, která může vést až ke smrti hostitele..
V tomto komplexu našli novou složku, která se v buňkách jiných organismů nevyskytuje. Vzhledem k tomu, že objevený komplex má pro fungování buňky zásadní význam, může se stát klíčem pro další vývoj slibných látek na léčbu spavé nemoci.
Mitochondrie fungují v buňce jako minielektrárny – vyrábějí energii v podobě chemické sloučeniny adenosintrifosfátu (ATP), který slouží jako palivo pro průběh jiných reakcí v buňce. ATP se „vyrábí“ při procesu buněčného dýchání na vnitřní mitochondriální membráně pomocí bílkovinného komplexu FoF1-ATP syntáza, který slouží jako rotační turbína.
Aktivita této turbíny je v buňce nezastupitelná, a proto její struktura a funkce zůstávají striktně konzervativní a neměnné u buněk většiny organismů. Vědci však zjistili, že u studovaného parazita Trypanosomy brucei, je tomu jinak.
„Už prvotní tomografické studie mitochondrií Trypanosomy brucei odhalily, že komplex F1-ATPázy se vymyká. Po několikaleté intenzivní experimentální práci jsme nakonec získali krystalickou strukturu tohoto komplexu v atomickém rozlišení a tuto domněnku jsme s naprostou určitostí potvrdili,“ říká Alena Zíková z Parazitologického ústavu BC AV ČR. Zatímco u většiny organismů se daný komplex skládá výhradně z pěti stavebních kamenů (podjednotek a, β, g, d, e), u studovaného parazita obsahuje komplex F1-ATPázy ještě šestou unikátní podjednotku.
„Naše studie vyvrací dlouhodobé dogma o neměnném a konzervativním složení podkomplexu F1-ATPázy,“ dodává Alena Zíková s tím, že objev může posloužit medicínským účelům. Díky tomu, že má tento komplex v buňce parazita nezbytnou a nezastupitelnou roli a zároveň se výrazně odlišuje od stejného komplexu u buněk člověka, představuje slibnou substanci pro vývoj nových léčivých látek.
Tyto látky mohou být využity nejen k léčbě spavé nemoci, ale také dalších lidských onemocnění způsobených příbuznými druhy T. brucei, a to leishmániemi a parazitem Trypanosoma cruzi.
Práce byla publikována v prestižním mezinárodním časopise Proceedings of the National Academy of Sciences of the United States of America v únoru 2018.